







《人教版化学20版必修二7.3.1《乙醇与乙酸有机化合物PPT乙醇》PPT课件》是由用户上传到老师板报网,本为文库资料,大小为2.15 MB,总共有50页,格式为pptx。授权方式为VIP用户下载,成为老师板报网VIP用户马上下载此课件。文件完整,下载后可编辑修改。
- 文库资料
- 50页
- 2.15 MB
- VIP模板
- pptx
- 数字产品不支持退货
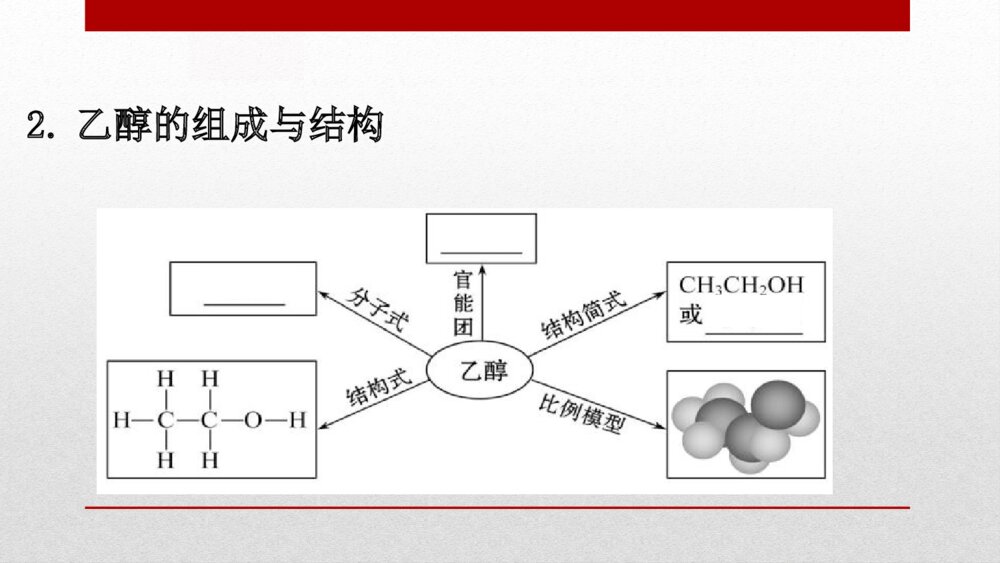
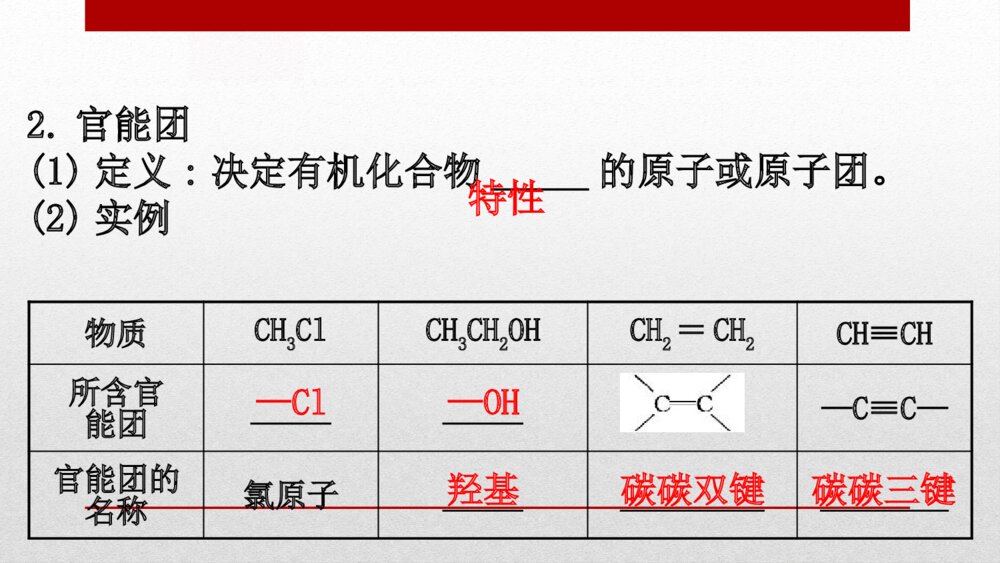
第七章 有机化合物第三节 乙醇与乙酸第1课时 乙醇一、乙醇的物理性质与组成和结构1.乙醇的物理性质俗称颜色气味密度溶解性挥发性酒精______________比水的___能与水以任意比_____,易溶于有机溶剂_______无色特殊香味小互溶易挥发2.乙醇的组成与结构【巧判断】(1)乙醇的结构简式为C2H5OH,说明乙醇分子中共有两种氢原子。( )提示:×。乙醇分子中有三种氢原子,其中烃基上的氢原子有两种,羟基上有一种。(2)乙醇的分子结构中有OH-。( )提示:×。乙醇结构中没有OH-而是羟基(—OH)。(3)羟基的电子式为H。( )提示:×。羟基的电子式为H。【情境·思考】俗话说“酒香不怕巷子深”,意思就是说如果酒酿得好,就是在很深的巷子里,也会有人闻香知味,前来品尝。这里面体现了乙醇的哪些物理性质?提示:俗语中体现了乙醇是一种易挥发的有香味的液体。二、烃的衍生物与官能团1.烃的衍生物烃分子中的_______被其他原子或原子团所取代而生成的一系列化合物。如一氯甲烷、1,2-二溴乙烷、乙醇、乙酸等。氢原子2.官能团(1)定义:决定有机化合物_____的原子或原子团。(2)实例物质CH3ClCH3CH2OHCH2=CH2CH≡CH所含官能团__________—C≡C—官能团的名称氯原子______________________特性—Cl—OH羟基碳碳双键碳碳三键【巧判断】(1)乙烯的官能团是碳碳双键,乙烷的官能团是碳碳单键。( )提示:×。乙烷中没有官能团。(2)乙醇的官能团是OH-。( )提示:×。官能团均为电中性基团,乙醇的官能团是羟基(—OH)不是OH-。三、乙醇的化学性质与用途1.乙醇与Na反应实验操作实验现象①钠开始沉于试管底部,最终慢慢消失,产生___________气体;②烧杯内壁有_____产生;③向烧杯中加入澄清石灰水_________实验结论乙醇与钠反应生成__,化学方程式为_____________________________无色可燃性水珠不变浑浊H22CH3CH2OH+2Na→2CH3CH2ONa+H2↑2.乙醇的氧化反应(1)燃烧①化学方程式:__________________________。②现象:产生淡蓝色火焰,放出_________。CH3CH2OH+3O22CO2+3H2O大量的热点燃(2)催化氧化(3)与强氧化剂反应反应原理:CH3CH2OH_______。CH3COOH【巧判断】(1)乙醇与金属钠反应时,是乙醇分子中羟基中的O—H键断裂。( )提示:√。乙醇与金属钠反应生成乙醇钠,是乙醇分子中羟基中的O—H键断裂。(2)检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水。( )提示:√。检验乙醇中是否含有水可用无水硫酸铜检验,若变蓝则表明乙醇中含水。(3)甲烷、乙烯、苯、乙醇都是无色不溶于水的有机化合物。( )提示:×。甲烷、乙烯、苯都不溶于水,但乙醇却能与水以任意比例互溶。【情境·思考】银饰作为我国传统的一种首饰,一直以来都广受人们的喜爱。焊接银器、铜器时,表面会生成黑色的氧化膜,银匠说可以先把铜、银放在火上烧热,马上蘸一下酒精,铜、银会光亮如初。这一过程中发生了哪些反应?铜在反应中起到了什么作用?提示:2Cu+O22CuO,CH3CH2OH+CuOCH3CHO+Cu+H2O,铜作为催化剂。3.乙醇的用途(1)用作酒精灯、火锅、内燃机等的燃料。(2)用作生产医药、香料、化妆品、涂料等的化工原料。(3)医疗上常用体积分数为____的乙醇溶液作消毒剂。75%知识点 从化学键、官能团的角度认识乙醇的化学性质【重点释疑】1.乙醇的结构与化学键的断裂情况乙醇的性质键的断裂与钠反应断①键燃烧断①②③④⑤键催化氧化断①③键2.乙醇与钠反应的位置和方式【注意】(1)乙醇与钠的反应比水与钠的反应要缓和得多,这说明乙醇分子羟基中的氢原子不如水分子中的氢原子活泼。(2)1mol乙醇与足量钠反应,产生0.5molH2,该关系可延伸为1mol羟基(—OH)跟足量钠反应产生0.5molH2。3.乙醇催化氧化的过程(1)将弯成螺旋状的铜丝灼烧,铜丝表面变黑色。2Cu+O22CuO(2)将灼烧后的铜丝插入乙醇中,铜丝表面由黑变红。总方程式2C2H5OH+O22CH3CHO+2H2O(3)醇的催化氧化反应规律醇在有催化剂(铜或银)存在的条件下,可以发生催化氧化反应生成醛,但并不是所有的醇都能被氧化生成醛。①凡是含有R—CH2OH(R代表烃基)结构的醇,在一定条件下都能被氧化成醛;2R—CH2OH+O22R—CHO+2H2O。②凡是含有结构的醇,在一定条件下也能被氧化,但生成物不是醛,而是酮()。③凡是含有结构的醇通常情况下不能被氧化。【思考·讨论】(1)所有的醇类物质均能与金属钠反应放出氢气吗?提示:所有醇类物质都有羟基,因此都能与钠反应放出氢气。(2)根据乙醇催化氧化的实质,推测的催化氧化产物是什么,能被催化氧化吗?【案例示范】【典例】乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法中不正确的是( )A.和金属钠反应时键①断裂B.在铜或银催化共热下与O2反应时断裂①和③C.在铜或银催化共热下与O2反应时断裂①和⑤D.在空气中完全燃烧时断裂①②③④⑤【解题指南】解答本题的关键是掌握乙醇在不同反应中化学键的断键情况、反应方式。【解析】选C。乙醇与钠反应生成乙醇钠,是羟基中的O—H键断裂,A正确;乙醇催化氧化生成乙醛时,断裂①和③化学键,B正确,C错误;乙醇完全燃烧时化学键①②③④⑤全部断裂,D正确。【母题追问】“固体酒精”也称固化酒精,因使用、运输和携带方便,燃烧时对环境的污染较少,与液体酒精相比比较安全,作为一种固体燃料,广泛应用于餐饮业、旅游业和野外作业等。思考:(1)固体酒精是酒精的固态形式吗?提示:不是。固体酒精也被称为“酒精块”或固体燃料块。固体酒精并不是固体状态的酒精(酒精的熔点为-117.3℃,纯净物常温下是液体),而是将工业酒精(主要成分为乙醇,CH3CH2OH)中加入凝固剂[可使用(CH3COO)2Ca]使之成为固体形态。(2)将铜制火锅置于固体酒精的火焰上灼烧,发现锅底并未变黑,试结合有关知识加以解释。提示:铜在空气中加热时会被氧化为黑色的氧化铜,但是氧化铜可以被挥发出的乙醇还原重新反应生成铜。故铜锅底不一定变黑。【迁移·应用】1.某有机物的结构简式为。下列关于该有机物的叙述中,不正确的是( )A.能与金属钠发生反应并放出氢气B.能在催化剂作用下与H2发生加成反应C.不能使酸性KMnO4溶液褪色D.在铜作催化剂条件下能发生催化氧化反应生成醛【解析】选C。该有机物分子中含有、—OH两种官能团,其中—OH能和Na反应放出H2,能在铜作催化剂条件下发生催化氧化反应生成醛;能使酸性KMnO4溶液褪色,能在催化剂作用下与H2发生加成反应。故C不正确。2.下列四种有机物的分子式都是C4H10O,其中不能被氧化为同碳原子数醛的是( )A.①和②B.②和③C.③和④D.①和④【解析】选D。醇分子结构中与—OH相连的碳原子上至少要有一个氢原子才能发生催化氧化反应。—OH连在链端碳原子上的醇,即R—CH2OH结构的醇,可被催化氧化为醛,亦可被强氧化剂氧化为酸。2R—CH2OH+O22R—CHO+2H2O。【补偿训练】催化氧化的产物是的醇是( )【解析】选A。醇发生催化氧化反应时,只与分子中的—CH2OH原子团有关,与其他基团无关,则根据题干产物结构式得被氧化的醇为。【素养提升】酒的主要成分是乙醇,少量饮酒对人体有益,但酗酒有害健康。科学研究表明酒量的大小与人体内某些酶有关。(1)乙醇是无色有特殊香味的液体,工业上用乙烯与水反应可制得乙醇,写出该反应的化学方程式并判断反应类型。提示:CH2=CH2+H2OCH3CH2OH,加成反应。(2)阅读材料分析乙醇在人体内的变化,写出涉及的化学方程式。提示:2CH3CH2OH+O22CH3CHO+2H2O;2CH3CHO+O22CH3COOH;CH3COOH+2O2→2CO2+2H2O。【课堂回眸】



















